林豊益 特聘教授 | 生命科學系
現為本校生命科學系特聘教授,專長是魚類環境生理與毒理學,特別是探討環境中危害物質如何影響到水生魚類的生理運作。實驗室利用斑馬魚與青鱂魚為模式物種,探討環境危害物質如何影響魚類胚胎或是成體之各種生理功能。實驗室也致力於建立斑馬魚的檢測技術、疾病模式,並應用於測試藥物的生物活性,探討藥物的作用機轉。


【本篇報導由生命科學系 林豊益特聘教授研究團隊提供】
順鉑(cisplatin)是一種常見的化療藥物,但它可能引起腎毒性,這對治療造成限制。同時,順鉑排放進入水環境,也可能對魚類造成損害。為了解決這些問題,林豊益教授團隊使用斑馬魚胚胎研究了順鉑對胚胎離子細胞的損害機制。研究團隊發現,順鉑對胚胎的毒性與暴露濃度和時間有相關性,導致離子細胞數量和功能受損。這種損害與抗氧化和細胞凋亡基因的表現有關,增加了細胞氧化壓力、損害粒線體,以及促進細胞凋亡。這個研究模型可用於篩選測試能減輕順鉑腎毒性的藥物。
順鉑是一種廣泛使用的化療藥物,可有效對抗多種癌症。然而,它經常會引起腎毒性副作用,導致病人腎功能受損,限制其治療效果。因此,了解順鉑引起腎毒性的機制對於開發可減輕其不良反應的新療法非常重要。此外,環境研究發現順鉑可能被排放到水體中,主要來源包括醫療設施的廢水排放和患者排泄。這些排放源可以將順鉑引入自然水體,如河流、湖泊和海洋。這些水中的順鉑污染可能對水生生物造成損害,包括魚類。
基於上述原因,研究順鉑化療藥物如何對魚類產生細胞毒性的機轉,並試圖找出能減低其毒性的方法,將有助於解決臨床上腎毒性的副作用,並評估其對環境的風險。林豊益教授團隊利用斑馬魚胚胎為模型,研究順鉑如何傷害胚胎離子細胞這種腎毒性疾病模式。研究發現胚胎在暴露於順鉑後,會出現濃度與暴露時間依賴性毒性影響,包括離子細胞的數量與功能的損傷。這些細胞傷害是透過影響一些抗氧化和細胞凋亡基因的表現,使得細胞氧化壓力增加、粒線體損傷、以及細胞凋亡機轉所產生(如圖1)。該研究模型可以應用於測試並篩選能改善順鉑引起腎毒性的藥物。
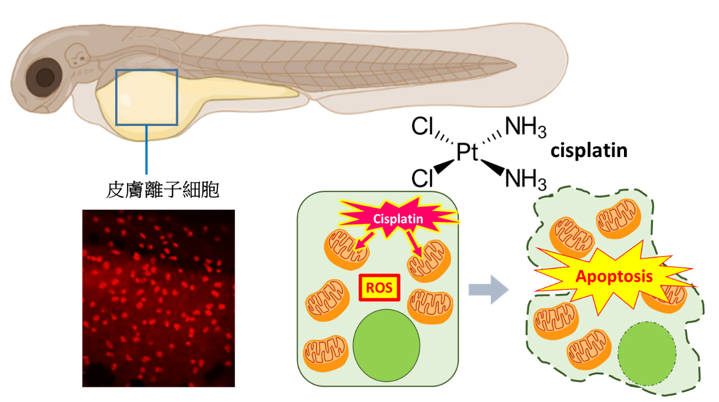
圖1:順鉑(cisplatin)造成胚胎皮膚離子細胞的損傷機轉。離子細胞(ionocyte)為富含粒線體的細胞,功能與人類腎臟細胞類似。在順鉑的作用下,細胞內粒線體會受損,活性氧(ROS)增加,進而導致細胞凋亡(apoptosis)。
原文出處:Hung, G. Y., Wu, C. L., Motoyama, C., Horng, J. L., & Lin, L. Y. (2022). Zebrafish embryos as an in vivo model to investigate cisplatin-induced oxidative stress and apoptosis in mitochondrion-rich ionocytes. Comparative Biochemistry and Physiology Part - C: Toxicology and Pharmacology,259, Article 109395.https://doi.org/10.1016/j.cbpc.2022.109395

現為本校生命科學系特聘教授,專長是魚類環境生理與毒理學,特別是探討環境中危害物質如何影響到水生魚類的生理運作。實驗室利用斑馬魚與青鱂魚為模式物種,探討環境危害物質如何影響魚類胚胎或是成體之各種生理功能。實驗室也致力於建立斑馬魚的檢測技術、疾病模式,並應用於測試藥物的生物活性,探討藥物的作用機轉。