【本篇報導由化學系 李以仁副教授研究團隊提供】
細胞中的三核苷酸重複序列容易自行摺疊成髮夾結構,干擾DNA複製與修復,導致重複序列異常擴張,與多種神經退化疾病密切相關。人類複製蛋白A(hRPA)是細胞內最豐富的單股DNA結合蛋白,理論上應能解開這類有害結構,然而其與三核苷酸重複序列的髮夾的互動機制至今未明。
本研究以單分子螢光共振能量轉移技術,即時追蹤hRPA解開CTG三核苷酸重複序列髮夾的過程。結果顯示,髮夾末端需有單股尾巴作為初始結合位點,hRPA才能啟動打開髮夾結構的過程;此過程並非一步完成,而是透過不同結合域分步推進。這個逐步機制會週期性暴露短暫的單股懸臂,而CTG序列特有的滑動重組特性會驅使懸臂迅速重新摺疊為平頭髮夾,使進度一再受阻。
此外,完整打開較長髮夾所需的hRPA濃度呈非線性暴增,當重複數達病理相關長度時,所需濃度可能超越細胞生理範圍,致病髮夾因而難以在體內被有效清除。
本研究揭示hRPA的動態分步結合與CTG滑動重組之間的競爭機制,為病理性重複擴張在細胞中持續累積提供了分子層次的解釋,並為未來開發干預策略指出方向。
我們的基因組並不總是安分守己。在某些神經退化疾病患者體內,序列會像失控的影印機,將同樣的三個字母反覆複製,愈積愈多,最終釀成災禍。這種三核苷酸重複序列擴張是強直性肌肉失養症、脊髓小腦萎縮症等疾病的根源。然而,細胞備有保護蛋白質,為何仍無法阻止這場基因災難?
臺師大李以仁副教授團隊匡玉琪同學等人,攜手臺大冀宏源教授的研究團隊,今年一月發表於美國國家科學院院刊(PNAS)的研究給出了答案:問題關鍵在於結構本身會趁隙溜走。
兩個主角,一場角力
第一個主角是重複序列形成的髮夾結構。當單股存在時,這類序列會自行摺疊成髮夾結構,干擾細胞複製與修復,促進異常擴張。
第二個主角是人類複製蛋白,細胞中含量最豐富的單股結合蛋白,負責穩定單股、防止異常結構形成,也能打開已存在的髮夾結構,應是對抗髮夾結構的最佳武器。
研究團隊以單分子螢光共振能量轉移技術,在分子層次即時觀察兩者互動,發現現實遠比想像複雜。
三個關鍵發現
第一,蛋白需要入口才能作業。當髮夾末端沒有突出的單股尾巴時幾乎無從下手,必須在高濃度下才能打開髮夾結構。
第二,逐步入侵反而留下破綻。研究人員為髮夾加上單股尾巴後,蛋白得以結合並開始解開髮夾,但並非一口氣完成,而是透過不同結合域逐步推進,每個階段都暫時暴露出一小段懸臂。問題正在這裡:重複序列擁有獨特的滑動重組能力,暴露的懸臂會迅速摺疊回平頭髮夾,讓入侵進度歸零。透過抑制滑動的對照實驗,研究團隊證實一旦阻斷滑動,蛋白在極低濃度下便能完成解析,效率遠優於正常序列。
第三,重複序列愈長,所需濃度呈非線性暴增。每多出一段重複,所需最低濃度便要提升數倍。當重複數達到病理相關長度時,所需濃度可能超越細胞生理範圍,防護機制形同失效。
一個更完整的致病模型
研究團隊提出分步模型(如圖1):蛋白先抓住單股尾巴,再像拉開拉鍊般逐域推進;但滑動本性讓已解開的部分一再反摺回平頭髮夾,形成頑強中間態。只有在高濃度下,第二個蛋白分子才能搶在滑動前抓住懸臂,協力完成解析。
這項研究解答了長期懸而未決的問題:為什麼即使細胞中存在大量保護蛋白,病理性擴張依然持續?答案是動態滑動與逐步解析之間的競爭,共同構成難以突破的屏障。重複序列一旦超過某個閾值,細胞防禦便會失效,這或許正是疾病症狀往往在擴張累積到一定程度後才急遽惡化的分子基礎。這項發現為未來治療指出潛在方向,例如開發抑制髮夾滑動的藥物,為這類仍缺乏根治方法的疾病帶來一線曙光。
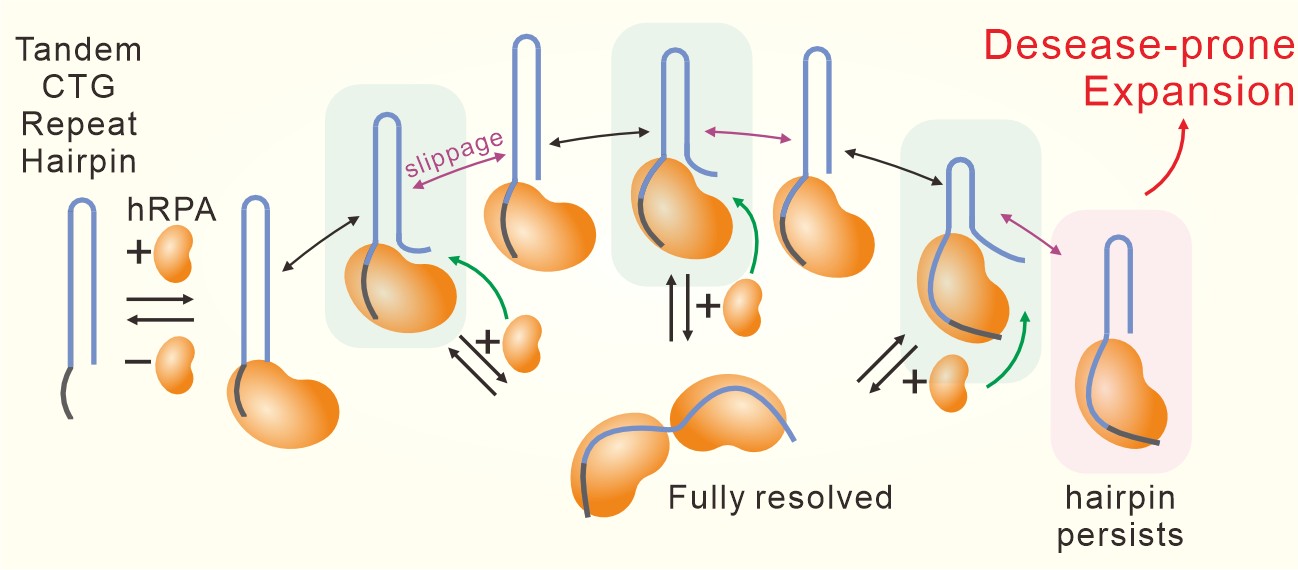
圖1:本研究分子機制模型示意圖
原文出處:Kuang, Y.-C.; Chen, S.-Y.; Chang, H.-Y.; Ni, C.-W.; Chi, P.; Lee, I.-R. Slippage Reconfiguration of Trinucleotide Repeat Hairpins Impedes Resolution by Human Replication Protein A. Proc. Natl. Acad. Sci. U.S.A. 2026, 123 (4), e2526355123. https://doi.org/10.1073/pnas.2526355123